Química > Orgânica > Reações - Condensação
Reação de condensação significa que duas moléculas se juntam para formar uma maior
O primeiro tipo de reação de condensação que estudaremos é extremamente importante: a formação da ligação peptídica:
Ligação peptídica
A ligação peptídica é de extrema importância porque sem ela não haveria proteínas, e portanto não haveria nenhum tipo de vida.
A reação abaixo, usando cores para melhor visualizar o que ocorre, indica a eliminação de água (condensação) na formação da ligação peptídica.
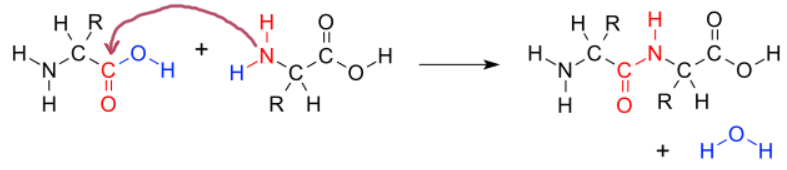
Reação de formação da ligação peptídica, entre 2 aminoácidos
Os 2 reagentes são aminoácidos genéricos, pois os radicais R- podem ser escolhidos dentre as 20 variedades. Perceba que ambos possuem um grupo funcional ácido e um amina. É mostrada a formação de apenas um pequeno peptídeo (2 aminoácidos apenas) , mas a reação pode prosseguir e agregar milhares de aminoácidos, como é o caso em muitas proteínas.
Eu fiz uma animação desta reação, para se entender melhor:
A reação ocorre entre o grupo funcional ácido e o amina. O nitrogênio da amina possui 1 par de elétrons solitário que é atraído pelo grupo carbono do grupo carbonila do ácido (seta na figura), onde há uma ausência de elétrons devido à presença da dupla ligação com o oxigênio. Para que se forme a ligação entre C e N, o grupo -OH ligado ao C sai fora, assim como um dos H ligados ao N. Ambos -OH e H liberados, se juntam para formar água.
A reação inversa é a hidrólise, onde a água volta e faz a quebra da ligação. Enzimas específicas são necessárias para que isso ocorra.
